Área Ambiental
Vol 11 Numero 1 del 2020
DOI: https://doi.org/10.22490/21456453.3081
Evaluación de coagulantes naturales en la clarificación de aguas
Evaluation of natural coagulants in water clarification
1sebastian Barreto Pardo, 2diana Karina vargas Moncada,3lida ruiz Martínez, 4sandra liliana gómez ayala
1Ingeniería Ambiental, Universidad Libre Sede Bosque Popular, Bogotá D.C- Colombia. 2Ingeniería Ambiental,Universidad Libre Sede Bosque Popular, Bogotá D.C- Colombia. 3Maestría en Gestión Ambiental, Universidad Libre Sede Bosque Popular, Bogotá D.C- Colombia. 4Doctorado en Química, Universidad Libre Seccional Campus Universitario Majavita, El Socorro Santander-Colombia.
1juans-barretop@unilibre.edu.co 2dianak-vargasm@unilibre.edu.co,3lidae.ruizm@unilibre.edu.co ,4sandral.gomeza@unilibre.edu.co.edu.co
Resumen
La coagulación/floculación y sedimentación de partículas presentes en el agua hacen parte del tratamiento primario avanzado, el cual es el más utilizado para la remoción de partículas contaminantes presentes en aguas con altos niveles de turbiedad. Es por esto, que en esta investigación se realizó la comparación entre el coagulante comercial más utilizado (sulfato de aluminio) y los coagulantes naturales extraídos de la semilla del aguacate y el mucílago del café para tratar las aguas de la quebrada La Guayacana ubicada en el municipio de El Socorro-Santander, para ello se realizaron ensayos de jarras y se determinó la eficiencia de cada uno de los coagulantes mencionados, en términos de reducción de color y turbiedad. Los resultados obtenidos señalan que el coagulante tipo C (semilla de aguacate) presentó una remoción del 44.27% en la turbiedad, por su parte el coagulante tipo B (mucílago del café y solución buffer de fosfato) fue el coagulante con mejores resultados y permitió remover el 64,29% de la turbiedad y 52,20% de color, indicando que este extracto puede servir como un coagulante preliminar o auxiliar en el proceso de tratamiento primario de aguas que presentan valores considerables en la turbiedad.
Palabras Clave: Color, Dosis Óptima, Ensayo de Jarras, Turbiedad.
Abstract
Coagulation / flocculation and sedimentation of particles present in the water are part of the advanced primary treatment, which is the most commonly used for the removal of contaminating particles present in waters with high turbidity levels. That is why, in this investigation, a comparison was made between the most commonly used commercial coagulant (aluminum sulfate) and the natural coagulants extracted from the avocado seed and the coffee mucilage to treat the waters of La Guayacana creek located in the municipality of El Socorro-Santander, for that purpose pitcher tests were carried out and the efficiency of each of the coagulants mentioned was determined, in terms of color and turbidity reduction. The results obtained indicate that the coagulant type C (avocado seed) presented a removal of 44.27% in turbidity, meanwhile the coagulant type B (coffee mucilage and phosphate buffer solution) was the coagulant with better results and allowed to remove 64.29% of the turbidity and 52.20% of color, indicating that this extract can serve as a preliminary or auxiliary coagulant in the process of primary water treatment that has considerable turbidity values.
Key Words: Color, Optima Dose, Trial of jars, Turbidity.
Resumen Gráfico
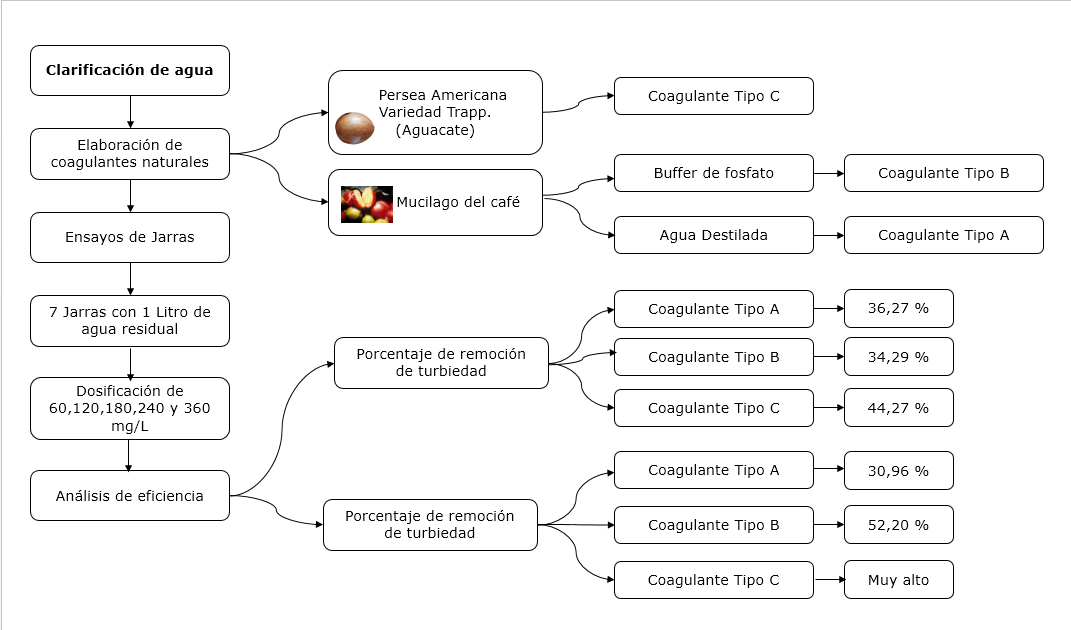
Figura 1. Resumen Gráfico. Fuente: Autores
INTRODUCCIÓN
En la actualidad, cada vez se fabrican más cantidades de productos lo que incrementa la producción de contaminantes tanto orgánicos como inorgánicos, los cuales en muchas oportunidades son liberados indiscriminadamente al ambiente, en particular a las aguas superficiales (Yin, 2010). No obstante, las aguas pueden ser tratadas mediante procesos de coagulación, floculación y sedimentación para la remoción de material suspendido o coloidal, sin embargo, esto conlleva al aditamento de más sustancias químicas al efluente, para así lograr la remoción de turbidez, la cual es un indicador de la presencia de los sólidos en el agua (Kakoi, Kaluli, Ndiba, & Thiong’o, 2016).
El tratamiento primario avanzado de aguas residuales consiste en la combinación de los procesos de coagulación/floculación/sedimentación y representa una etapa esencial en el tratamiento de la mayoría de las aguas residuales. Debido a que, la existencia de material particulado remanente en el agua puede afectar los demás procesos para el tratamiento de aguas residuales, entre ellos el proceso de desinfección aumentando el riesgo de propagación de enfermedades transmitidas por el agua (Bina, Mehdinejad, Nikaeen, & Attar, 2009). Por otro lado, las sustancias utilizadas en la etapa coagulación/floculación pueden clasificarse en dos, polímeros sintéticos y naturales, dentro de los polímeros sintéticos se encuentran algunos derivados de la poliacrilamida y el polietileno, estos generalmente son poco usados debido a la presencia de monómeros residuales los cuales son neurotóxicos y carcinógenos. Por su parte, los polímeros naturales obtenidos a partir de microorganismos, tejidos y semillas de plantas o animales son biodegradables y seguros para la salud humana (Ramírez Arcila, Jhoan, & Peralta, 2015). Los coagulantes de mayor uso son de origen químico, generalmente sales de metales trivalentes, entre estos se puede mencionar las sales de aluminio y de hierro (M. Šćiban, Klašnja, Antov, & Škrbić, 2009). Las sales de aluminio se han asociado con la enfermedad de Alzheimer y otras enfermedades neurológicas, conforme a algunos estudios demuestran cómo el cuerpo humano asimila fácilmente el aluminio y da lugar a consecuencias negativas a largo plazo; lo anterior teniendo en cuenta que una concentración de aluminio superior a 0,1 ppm en agua para consumo humano puede ser un factor de riesgo para la salud humana (Parra et al., 2011). Por su parte las consecuencias adversas por el uso de sales inorgánicas en el tratamiento del agua pueden variar desde la generación de altos volúmenes de desechos inorgánicos potencialmente tóxicos, los cuales requieren la eliminación apropiada (Abebe, Chen, & Sobsey, 2016); cambios en el pH del agua e ineficacia de los mismos a baja temperatura (Shamsnejati, Chaibakhsh, Pendashteh, & Hayeripour, 2015).
Con base en lo anterior, existe un interés creciente en aprovechar los polímeros orgánicos obtenidos a partir de extractos de plantas o sus semillas para la coagulación/floculación en el tratamiento de aguas debido a su nula toxicidad y a su alta biodegradabilidad, motivo por el cual este tipo de extractos son comúnmente llamados coagulantes naturales (Abebe et al., 2016). La aplicación de coagulantes de este tipo constituye un gran esfuerzo en la búsqueda de cumplir con las iniciativas globales de desarrollo sostenible, el mundo se encuentra en la era del cambio climático, el agotamiento de los recursos naturales y la degradación ambiental deben ser frenadas con la implementación de la tecnología ambiental sostenible (Yin, 2010). Por lo tanto, es deseable desarrollar alternativas ambientalmente aceptables y económicamente viables para reemplazar los coagulantes sintéticos. Teniendo en cuenta que las plantas pueden cultivarse localmente, los coagulantes naturales a base de plantas resultarían ser más rentables que los productos químicos importados.
Existen diversos precedentes con relación al uso de diferentes coagulantes obtenidos de plantas, Prospero Alpino (botánico italiano) ofrece un testimonio del uso de almendras para ayudar a la sedimentación, en este caso se empleó cáscara de almendras dulces y aplastadas para la clarificación del agua, haciendo las veces de ayudante de sedimentación. Por otro lado, Felix D’Acret escribió un notable documento en el que describe la filtración a través de recipientes porosos y la coagulación con almendras y frijoles en la clarificación del agua para la potabilización (Fatombi, Lartiges, Aminou, Barres, & Caillet, 2013). De igual modo, en la actualidad se hace frecuente la búsqueda de otros compuestos orgánicos de origen natural para la fabricación de coagulantes, como por ejemplo las cáscaras de naranja (Kebaili, Djellali, Radjai, Drouiche, & Lounici, 2018), las del banano (Kakoi et al., 2016), las semillas de habas (Kukić, Šćiban, Prodanović, Tepić, & Vasić, 2015), los almidones (Choy, Prasad, Wu, Raghunandan, & Ramanan, 2016), las castañas y bellotas (M. Šćiban et al., 2009), las legumbres (M. B. Šćiban, Klašnja, & Stojimirović, 2005) entre otros. Sin embargo, la mayoría de las revisiones sobre coagulantes naturales, hacen hincapié principalmente en cuatro plantas, la semilla de la Moringa Oleífera, la semilla de Nirmali, los taninos y el cactus Opuntia Ficus-Indica empleados para el tratamiento de agua bruta y residual (Yin, 2010).
Por otro lado existen precedentes donde se afirma que los taninos catiónicos pueden ser empleados como agentes de coagulación, dado que a partir de estos es posible sintetizar coagulantes partiendo de varias materias primas (Beltrán-Heredia, Sánchez-Martín, & Gómez-Muñoz, 2010), en especial extractos de diferentes semillas como "Horse chestnut" (Aesculus hyppocastanum), roble común (Q. robur), roble turco (Q. cerris), roble rojo norteño (Q. ruber) y castañea europea (C. sativa) a las cuales les determinaron el contenido de proteínas y su actividad coagulante, encontrando que la castaña europea y el roble común son las más eficientes (M. Šćiban et al., 2009). Por otro lado, también se han empleado extractos etanólicos de las semillas de uvas (GSE) y polifenoles derivados de las mismas, como ácido tánico y la catequina en un esfuerzo por encontrar nuevos coagulantes orgánicos naturales (NOCs) (Jeon et al., 2009). También, se han investigado polímeros catiónicos comerciales a base de taninos (TBP) con el objeto de establecer sus propiedades químicas básicas y su comportamiento como coagulante (Graham, Gang, Fowler, & Watts, 2008).
Adicional a ello algunos investigadores analizaron la aplicación de taninos como coagulantes primarios y/o ayudantes de la coagulación en el tratamiento de agua, el tanino en estos estudios fue extraído de la Valonia (Özacar & Şengil, 2002; Yin, 2010). El estudio permitió concluir que el tanino combinado con el sulfato de aluminio es un excelente sustituto de los coagulantes químicos, debido a la cationización de los taninos (Beltrán-Heredia, Sánchez-Martín, & Dávila-Acedo, 2011) hecho que se debe a que los agentes coagulantes cargados positivamente pueden desestabilizar coloides aniónicos una vez se mezclan en soluciones acuosas provocando la remoción de una amplia variedad de sustancias aniónicas, tales como colorantes, tensoactivos y materia orgánica (Beltrán-Heredia et al., 2010). La semilla de aguacate empleada en el presente estudio posee material celular irregular que contiene taninos (Gaviaria Mejía & Mejía Aguas, 2012) derivados de la familia del ácido gálico y son los llamados hidrolizables, que poseen diversos efectos en sistemas biológicos, tales como atrapar y encapsular metales, actividad antioxidante y ayudante de precipitación, entre otras (Segovia Gomez, 2015).
Con respecto al mucilago de café, este se localiza entre la pulpa y la cáscara de la semilla de café y representa alrededor del 5% del peso de este. Adicionalmente, el mucílago es un sistema coloidal líquido, liofilico que actúa como un hidrogel, químicamente estos contienen agua, azúcares, ácidos orgánicos y pectinas. La estructura del mucílago presenta una primera fracción en donde se encuentran las pectinas, con propiedades gelificantes y una segunda fracción sin propiedades gelificantes (Braham & Bressani, 2017) otros autores (Goycoolea & Cárdenas, 2003; Matsuhiro, Lillo, Sáenz, Urzúa, & Zárate, 2006; Medina-Torres, Brito-De La Fuente, Torrestiana-Sanchez, & Katthain, 2000) afirman que los mucílagos son carbohidratos de naturaleza compleja que contienen L-arabinosa, D-galactosa, L-ramnosa y D-xilosa, así como ácido D-galacturónico en diferentes proporciones, este último siendo la estructura básica de las pectinas (Sociedad Latinoamericana de Nutrición, Sangronis, & Unai, 2008).
El principal uso de las pectinas en la industria alimentaria es como gelificante, espesante, texturizante, emulsificante y estabilizante, su aplicación más común es en la manufactura de mermeladas y jaleas. Esta funcionalidad de la pectina es atribuida a la presencia de regiones polares y apolares dentro de su molécula, lo que permite incorporarla a diferentes sistemas alimenticios (Sociedad Latinoamericana de Nutrición et al., 2008). Como se ha indicado, el mucílago del fruto del café es muy rico en sustancias pécticas que se podrían aislar. Sin embargo, estas sustancias son difíciles de recuperar debido a que el despulpado y lavado son operaciones inherentes al proceso de la extracción del café (Aritizábal Arias & Duque Orrego, 2005).
MATERIALES Y MÉTODOS
El proyecto fue desarrollado en el laboratorio de aguas y microbiología de la Universidad Libre seccional Socorro, Santander. Se realizó un muestreo puntual en el vertimiento en la quebrada La Guayacana del municipio de El Socorro; adicional a ello, para la extracción de los coagulantes se utilizó la semilla de aguacate, la cual representa un residuo que en su composición química posee taninos, los cuales pueden ser empleados como coagulantes (Beltrán-Heredia et al., 2010). Por su parte, el mucílago de café fue obtenido de la planta de beneficio que se encuentra en la Universidad Libre, el mucilago constituye un residuo que se genera en el proceso del descerezado y lavado en la producción del café. Para poder tener un punto de comparación en el estudio, se realizaron ensayos con un coagulante comercial “Sulfato de aluminio tipo B” y con ellos se evaluó el desempeño en la clarificación de los coagulantes convencionales con respecto a los usados en esta investigación, cabe resaltar que todos los coagulantes fueron preparados a una concentración del 2% (m/v).
Obtención de Coagulantes Naturales: en la extracción de los hidrocoloides (mucílago), se utilizó una mezcla acuosa de mucílago relación 3:1, tomada de la planta de beneficio de café del campus Majavita de la Universidad Libre, dicha mezcla pasó a través de un filtro de acero inoxidable de 2,38 mm y se dejó decantar en conos Imhoff durante 24 horas. Posteriormente se separó el agua del mucilago, y este último se dividió en dos partes, a la primera de ellas fue secada (50ºC; 40 min) y se dejó fermentar por un día más (Sáenz et al., 2006), la solución para este coagulante se preparó disolviendo 10 g de coagulante en 500 ml de agua destilada y se rotuló como coagulante tipo (A); la segunda porción del extracto se le realizó un tratamiento térmico en plancha (97ºC; 1 hora) y en horno secador por convención (50ºC; 1 hora y media) y se obtuvo un polvillo aproximadamente un tamaño de partícula de 1 mm; la solución para este primer coagulante se preparó disolviendo 10 g de coagulante en polvo en 500 ml de solución amortiguadora o buffer de fosfato y se rotuló como coagulante tipo (B).
Para el último coagulante, se utilizó la especie vegetal denominada Persea americana, variedad Trapp (Aguacate) presente en la zona. La semilla del aguacate fue triturada y se cernió con un tamiz de numero de malla 10 (2 mm U.S. Standar Sieve). Posteriormente, se llevó a un sistema de extracción Soxhlet durante 6 horas, se empleó éter etílico para la extracción del aceite de la semilla (ISPC, 1990) y finalmente se secó el extracto sólido en el horno secador por convección, es decir, el ripio de la semilla de aguacate a la cual le fue retirado el aceite. Para concluir, se pulverizó el ripio de semilla de aguacate a fin de obtener un polvo fino (Lizbeth & Meneses, 2015) con un tamiz de numero de malla 30 (0,500 mm U.S. Standar Sieve). La solución para este coagulante se preparó disolviendo 10 g de ripio de aguacate en 500 ml de agua destilada y se rotuló como coagulante tipo (C).
Prueba de jarras: Para determinar la eficiencia de los coagulantes, se realizó la prueba de jarras estándar, para tal fin se emplearon 7 jarras de un litro con agua residual, una se utilizó como jarra de control y las otras 6 fueron dispuestas en un floculador con velocidad de agitación variable. Cada una de estas jarras fue dosificada con los coagulantes obtenidos en concentraciones de 60, 120, 180, 240, 300 y 360 mg/L, los ensayos fueron realizados teniendo en cuenta el protocolo propuesto por (Shamsnejati et al., 2015), quienes establecieron el desarrollo del test de jarras mediante los etapas de dosificación, agitación rápida, agitación lenta y sedimentación, con replicas por triplicado, por ello todos los ensayos fueron realizados a una velocidad de agitación de 100 rpm para mezcla rápida durante 3 min y 40 rpm para mezcla lenta o floculación durante 15 min, la sedimentación se dio durante una hora y todos los ensayos fueron por triplicado.
Eficiencia y comportamiento de variables: Para analizar la eficiencia de los coagulantes en los respectivos ensayos, se determinó la turbiedad usando un turbidímetro (turbidímetro portable, HACH 2100Q, Colombia) y un espectrofotómetro (Fotómetro Spectroquant, NOVA 60 de Merck, Alemania) para la determinación del color, adicional a ello, se determinó el pH con la ayuda de un potenciómetro (Multímetro digital de dos canales, HACH HQ40D, Colombia) y la alcalinidad del agua mediante un proceso de titulación con un ácido y un indicador colorado (Chaibakhsh, Ahmadi, & Zanjanchi, 2014) y se calculó mediante la siguiente fórmula:
Donde,
- V indicador es el volumen (mL) de ácido sulfúrico utilizados en la titulación N es la normalidad del ácido sulfúrico utilizado
- V muestra es la alícuota de la muestra analizada
El porcentaje de remoción de color se determinó mediante la siguiente ecuación:
Donde,
- To es el valor inicial de la turbiedad
- Tf es el valor final de la turbiedad en cada ensayo
El porcentaje de remoción de color se determinó mediante la siguiente ecuación:
Donde,
- Co es el valor inicial de la turbiedad
- Cf es el valor final de la turbiedad en cada ensayo
Por otro lado, se determinó la dosis óptima de coagulante mediante las siguientes fórmulas:
Donde,
- Masa corresponde al valor en (mg) del coagulante a preparar
- Volumen es el valor en (mL) del coagulante a preparar
En donde,
- [Coagulante] es la concentración de coagulante determinada en la primera fórmula
- Va es equivalente al volumen (mL) aplicado en cada jarra en mililitros y corresponde al ensayo que se obtuvo en el test de jarras.
- Vm es el volumen de la muestra a tratar en Litros
Manejo de datos:
Se realizaron ensayos de jarras con los siguientes coagulantes: de sulfato de aluminio, mucílago de café con agua destilada (A), muciélago de café con solución buffer de fosfato (B) y semilla de aguacate (C); se hicieron mediciones de pH, color y turbiedad, adicionalmente se halló el porcentaje de remoción de turbiedad y color, teniendo en cuenta los parámetros iniciales que se muestran en la Tabla 1. Posteriormente se realizó el tratamiento de datos mediante la herramienta de Microsoft Excel, promediando cada uno de los datos obtenidos, puesto que se hicieron tres ensayos de jarras por coagulante, finalmente se procede a hallar la desviación estándar de color y turbiedad para cada uno de los datos con su respectivo porcentaje.
RESULTADOS Y DISCUSIÓN
Las condiciones iniciales de la calidad del agua residual se presentan en la Tabla 1. En esta se observa que la alcalinidad residual es menor a 100 mg de CaCO3/L hecho por el cual no se requirió la adición de alcalinizante para lograr la aglomeración de partículas (Arenas Esteves, 2017). Cabe resaltar que en los casos en los cuales el agua no contiene la alcalinidad suficiente para reaccionar con el coagulante generalmente se hace necesario añadir cal o hidróxido de sodio al agua (Giraldo & Castrillón Bedoya, 2012). Por otro lado, se realizó un único muestro puntual del vertimiento, obteniendo valores de 155 NTU y 177,5 UPC para la turbiedad y el color, dicho muestreo se realizó en el mes de octubre, en temporada de alta precipitación.
Tabla 1. Parámetros iniciales de calidad del agua residual empleada.
| Parámetro |
Valor |
UNIDAD |
|
pH |
6,9 |
- |
|
Alcalinidad |
154,9 |
mg de CaCO3/L |
|
Turbiedad |
155 |
UNT |
|
Color |
177,5 |
UPC |
Fuente de consulta: Autores
Las figuras 2 y 3 presentan la variación del porcentaje de remoción de turbiedad y color para los distintos coagulantes ensayados a distintas dosis. Se puede apreciar que el coagulante comercial permitió alcanzar los mayores porcentajes de remoción de turbiedad (99%±0,40) y de color (90%±1,19), valores consecuentes con otros autores como Sandoval y Canepa (Sandoval Arreola & Canepa Laines, 2014) quienes alcanzaron un 96,60% y un 98,32%, al igual que Heber, Marina y Leonardo (De Paula, De Oliveira Ilha, & Andrade, 2014) quienes afirmaron que el sulfato de aluminio por sí solo, cumple todas la especificaciones para tratar aguas grises con fines de reutilización, hecho que denota la alta efectividad de esta sal inorgánica en el tratamiento de agua residual y cruda. Por su parte, el coagulante extraído de mucilago de café, logró remover el 65% de turbiedad y un 30% de color con un margen de error de 2,47% y del 3,97% respectivamente, con una dosis óptima de 300 mg/L, lo cual y de acuerdo a distintos autores se debe a la acción de las cadenas pécticas en el proceso de aglomeración (Braham & Bressani, 2017) de partículas presentes en el agua de estudio.
Figura 2. Porcentaje de remoción de turbiedad vs.dosis de coagulante aplicado. Fuente de: Autores
Se observó que el efecto principal del coagulante tipo (A) es la remoción de turbiedad a pesar que permite remover color del agua, el porcentaje de remoción no es comparable con el de turbiedad. En la figura 2 se puede apreciar el comportamiento de los coagulantes, los porcentajes de remoción de turbiedad y su dosificación, observando que tanto el coagulante de mucilago tipo (A) y tipo (B) poseen cierta tendencia, sin embargo uno alcanza un nivel mayor de remoción que el otro. En la tabla 2 se presentan los resultados correspondientes a porcentajes de remoción y de turbiedad obtenidos con coagulantes similares a los empleados.
Tabla 2. Antecedentes Coagulantes Naturales
| Coagulante |
% Remoción de turbiedad |
Referencia |
|
Mucilago Cactus Opuntia Wentiana |
41,47 – 94,84 |
(Parra et al., 2011) |
|
Mucilago del cactus Stenocereus griseus |
14,5 - 80,42 |
(Fuentes S., Mendoza S, López M, Castro V., & Urdaneta M., 2011) |
|
Mucílago de fenogreco |
40 – 95 |
(Yin, 2010) |
|
Semilla de Malva |
||
|
Semilla Tamarindus indica |
Fuente: Los autores
Con respecto a los resultados presentados en la tabla 2 se puede afirmar que el coagulante tipo (A) se encuentra entre los rangos del porcentaje de remoción de turbiedad expuestos por los tres autores, lo que demuestra cierta tendencia en la actividad de los mucilagos en procesos de clarificación de aguas. Por otro lado, se puede afirmar que el coagulante tipo (B) fue poco efectivo en la reducción turbiedad y de color, arrojando valores entre 30% y 39% de remoción, con un intervalo de desviación aproximadamente del 0,4% y se detalla que este no alcanza ni el mínimo porcentaje de remoción (40%) en el que se encuentran los coagulantes mencionados anteriormente en la tabla. Cabe resaltar que los autores Anastasakis, Kalderis, & Diamadopoulos (2009) apoyaron el proceso de coagulación/floculación usando como coagulante sulfato de aluminio y como floculante mucilago de okra y de malva. Con el uso del primer floculante alcanzaron un 70% de remoción de turbidez y afirmaron que se eliminó un 19% más con respecto al coagulante por sí solo. Asimismo, con el uso del segundo floculante alcanzaron un porcentaje de remoción del 62% al 67%, siendo de un 5% a un 12% más efectivo que el coagulante por sí solo, lo que permite identificar una nueva metodología aplicable para el uso del coagulante tipo (A) y tipo (B) a fin de obtener mejores resultados.
Figura 3. Porcentaje de remoción de color vs dosis de coagulante aplicado. Fuente de: Autores
En la figura 3 se puede observar el comportamiento del porcentaje de remoción de color a medida que se realizan las dosificaciones, resaltando que el mejor comportamiento y el más efectivo en la reducción de color fue el del sulfato de aluminio. Por su parte el coagulante tipo C, no consiguió realizar remoción de color.
En el caso del coagulante tipo (C), presenta un mínimo porcentaje de remoción de turbiedad el cual osciló entre el 40% y 45%, en una variación de datos entre el 0,40% y 0,55% lo que indica su baja efectividad para el tratamiento de aguas.
Los taninos son compuestos orgánicos que favorecen el proceso de coagulación, de hecho indican que pueden ser utilizados como coagulantes primarios (Özacar & Şengil, 2002). Sin embargo, en esta ocasión su remoción en la clarificación de aguas fue baja resaltando que la semilla del aguacate es un fruto con una alta concentración de taninos (Braham & Bressani, 2017) . El uso de los taninos se encuentra muy arraigado en la industria textil al formar colorantes orgánicos a partir de estos (Devian & Saldarriaga, 2015). Nuevamente se hace evidente que los coagulantes ensayados no permiten alcanzar la efectividad que se logra con el sulfato de aluminio, pero sí pueden ser una alternativa para ayudar en el proceso de coagulación y disminuir la dosis del polielectrolito comercial.
CONCLUSIONES
En general el uso de coagulantes naturales permite una remoción tanto de turbiedad como de color en el agua residual a tratar, el leve aumento de pH permite suponer que no se requiere la adición de cal o hidróxido de sodio para lograr la coagulación de las partículas en el agua para su posterior aglomeración y sedimentación.
El coagulante obtenido a partir de mucilago de café en base tipo A, representa una alternativa para la clarificación del agua residual analizada dando lugar a una reducción significativa de turbiedad y color, sin embargo, los valores son inferiores a los que se logran con sulfato de aluminio
El aumento de color por efecto de ciertas sustancias en los extractos como en el caso del coagulante tipo B y tipo C puede ser eliminado por adsorción sobre carbón activado o por oxidación con peróxido de hidrógeno logrado reducir el color, materia orgánica y desinfección de agua residual después de la clarificación.
Literatura citada
Abebe, L. S., Chen, X., & Sobsey, M. D. (2016). Chitosan Coagulation to Improve Microbial and Turbidity Removal by Ceramic Water Filtration for Household Drinking Water Treatment. International Journal of Environmental Research and Public Health, 269. https://doi.org/10.3390/ijerph13030269
Anastasakis, K., Kalderis, D., & Diamadopoulos, E. (2009).Flocculation behavior of mallow and okra mucilage in treating wastewater. Desalination, 249(2), 786–791. https://doi.org/10.1016/j.desal.2008.09.013
Arenas Esteves, M. F. (2017). Formato guías de laboratorio. Guias de Laboratorio, 1–13.
Aritizábal Arias, C., & Duque Orrego, H. (2005). Caracterizacion De Beneficio De Café En Cinco Departamentos Cafeteros De Colombia. 56(4), 299–318.
Beltrán-Heredia, J., Sánchez-Martín, J., & Dávila-Acedo, M. A. (2011). Optimization of the synthesis of a new coagulant from a tannin extract. Journal of Hazardous Materials, 186(2–3), 1704–1712. https://doi.org/10.1016/j.jhazmat.2010.12.075
Beltrán-Heredia, J., Sánchez-Martín, J., & Gómez-Muñoz, M. C. (2010). New coagulant agents from tannin extracts: Preliminary optimisation studies. Chemical Engineering Journal, 162(3), 1019–1025. https://doi.org/10.1016/j.cej.2010.07.011
Bina, B., Mehdinejad, M. H., Nikaeen, M., & Attar, H. M. (2009). Effectiveness of chitosan as natural coagulant aid in treating turbid waters. Iranian Journal Of Environmental Health Science And Engineering, 6(4), 247–252.
Braham, J. E., & Bressani, R. (2017). Pulpa de cafe composición tecnologia y utilizacion. INCAP - Instituto de Nutrición de Centroamérica y Panamá (Vol. 91). Bogotá: Centro internacional de investigaciones para el desarrollo.
Chaibakhsh, N., Ahmadi, N., & Zanjanchi, M. A. (2014). Use of Plantago major L. as a natural coagulant for optimized decolorization of dye-containing wastewater. Industrial Crops and Products, 61, 169–175. https://doi.org/10.1016/j.indcrop.2014.06.056
Choy, S. Y., Prasad, K. N., Wu, T. Y., Raghunandan, M. E., & Ramanan, R. N. (2016). Performance of conventional starches as natural coagulants for turbidity removal. Ecological Engineering, 94, 352–364. https://doi.org/10.1016/j.ecoleng.2016.05.082
De Paula, H. M., De Oliveira Ilha, M. S., & Andrade, L. S. (2014). Concrete plant wastewater treatment process by coagulation combining aluminum sulfate and Moringa oleifera powder. Journal of Cleaner Production, 76, 125–130. https://doi.org/10.1016/j.jclepro.2014.04.031
Devian, J., & Saldarriaga, D. (2015). Pulverización de colorantes naturales por secado por atomización. Revista Universidad EAFIT, 41(137), 36–43.
Fatombi, J. K., Lartiges, B., Aminou, T., Barres, O., & Caillet, C. (2013). A natural coagulant protein from copra (Cocos nucifera): Isolation, characterization, and potential for water purification. Separation and Purification Technology, 116, 35–40. https://doi.org/10.1016/j.seppur.2013.05.015Fuentes S., L. D. C., Mendoza S, I. A., López M, A. M., Castro V., M. F., & Urdaneta M., C. J. (2011). Effectiveness of a coagulant extracted from Stenocerens griseus (Haw.) Buxb in water purification. Revista Tecnica de La Facultad de Ingenieria Universidad Del Zulia, 34(1), 48–56.
Gaviaria Mejía, M. A., & Mejía Aguas, M. C. (2012). Evaluación de la extracción de colorantes de la semilla de aguacate como negocio para la región antioqueña. Escuela de Ingeniería de Antioquia. Retrieved from http://www.dt.co.kr/contents.html?article_no=2012071302010531749001
Giraldo, M. D. L. A., & Castrillón Bedoya, D. (2012). Determinación de las dosis óptimas del coagulante sulfato de aluminio tipo b en función de la turbiedad y el color para la potabilización del agua en la planta de tratamiento de villa Santana. Universidad tecnológica de pereira.
Goycoolea, F. M., & Cárdenas, A. (2003). Pectins from Opuntia A Short Review. Journal of the Professional Association for Cactus Development, (February 2003), 17–29.
Graham, N., Gang, F., Fowler, G., & Watts, M. (2008). Characterisation and coagulation performance of a tannin-based cationic polymer: A preliminary assessment. Colloids and Surfaces A: Physicochemical and Engineering Aspects, 327(1–3), 9–16. https://doi.org/10.1016/j.colsurfa.2008.05.045
ISPC, I. de S. P. de C. (1990). Procecimiento para determinar materia grasa : Método Soxhlet. Sección Química de Alimentos, no2, 1–2. Retrieved from http://www.ispch.cl/lab_amb/met_analitico/doc/ambiente pdf/GrasSoxhlet.pdf
Jeon, J. R., Kim, E. J., Kim, Y. M., Murugesan, K., Kim, J. H., & Chang, Y. S. (2009). Use of grape seed and its natural polyphenol extracts as a natural organic coagulant for removal of cationic dyes. Chemosphere, 77(8), 1090–1098. https://doi.org/10.1016/j.chemosphere.2009.08.036
Kakoi, B., Kaluli, J. W., Ndiba, P., & Thiong’o, G. (2016). Banana pith as a natural coagulant for polluted river water. Ecological Engineering, 95, 699–705. https://doi.org/10.1016/j.ecoleng.2016.07.001
Kebaili, M., Djellali, S., Radjai, M., Drouiche, N., & Lounici, H. (2018). Valorization of orange industry residues to form a natural coagulant and adsorbent. Journal of Industrial and Engineering Chemistry. https://doi.org/10.1016/j.jiec.2018.03.027
Kukić, D. V., Šćiban, M. B., Prodanović, J. M., Tepić, A. N., & Vasić, M. A. (2015). Extracts of fava bean (Vicia faba L.) seeds as natural coagulants. Ecological Engineering, 84, 229–232. https://doi.org/10.1016/j.ecoleng.2015.09.008
Lizbeth, N., & Meneses, G. (2015). Evaluación de la semilla de Moringa Oleifera como coadyuvante en el proceso de coagulación para el tratamiento de aguas naturales del rio Bogotá en su paso por el municipio de Villapinzón, Cundinamarca.
Matsuhiro, B., Lillo, L. E., Sáenz, C., Urzúa, C. C., & Zárate, O. (2006). Chemical characterization of the mucilage from fruits of Opuntia ficus indica. Carbohydrate Polymers, 63(2), 263–267. https://doi.org/10.1016/j.carbpol.2005.08.062
Medina-Torres, L., Brito-De La Fuente, E., Torrestiana-Sanchez, B., & Katthain, R. (2000). Rheological properties of the mucilage gum (Opuntia ficus indica). Food Hydrocolloids, 14(5), 417–424. https://doi.org/10.1016/S0268-005X(00)00015-1
Özacar, M., & Şengil, I. A. (2002). The use of tannins from Turkish acorns (valonia) in water treatment as a coagulant and coagulant aid. Turkish Journal of Engineering and Environmental Sciences, 26(3), 255–263.
Parra, Y., Cedeño, M., María, G., Mendoza, I., Gonzáles, Y., & Fuentes, L. (2011). Clarificación de aguas de alta turbidez empleando el mucílago de opuntia wentiana (Brittton&Rose) / (Cactceae). Universidad Del Zulia; Ciencias Exactas , Naturales y Agropecuarias, Redieluz, 1, 27–33.
Ramírez Arcila, H., Jhoan, •, & Peralta, J. (2015). Agentes Naturales Como Alternativa Para El Tratamiento Del Agua Agents As Natural Alternative for Water Treatment. Facultad de Ciencias Básicas UMNG, 136–153. https://doi.org/10.18359/rfcb.1303
Sáenz, C., Berger, H., Corrales Garcia, J., Galletti, L., Garcia de Cortázar, V., Higuera, I., Varnero, M. T. (2006). Utilización agroindustrial del nopal. In C. Rosell (Ed.), Boletín de Servicios Agrícolas de la FAO. 162nd ed., p. 105.
Sandoval Arreola, M. M., & Canepa Laines, J. R. (2014). Moringa oleifera una alternativa para sustituir metálicos en el tratamiento de aguas superficiales, 17(2), 101.
Šćiban, M. B., Klašnja, M. T., & Stojimirović, J. L. (2005). Investigation of Coagulation Activity of Natural Coagulants From Seeds of Different Leguminose Species. Apteff, 36, 81–87. https://doi.org/10.2298/APT0536081S
Šćiban, M., Klašnja, M., Antov, M., & Škrbić, B. (2009). Removal of water turbidity by natural coagulants obtained from chestnut and acorn. Bioresource Technology, 100(24), 6639–6643. https://doi.org/10.1016/j.biortech.2009.06.047
Segovia Gomez, F. (2015). Aprovechamiento de residuos agro- industriales : Preparación de extractos , caracterización y uso en alimentos, 7. https://doi.org/10.1016/j.engstruct.2005.12.010
Shamsnejati, S., Chaibakhsh, N., Pendashteh, A. R., & Hayeripour, S. (2015). Mucilaginous seed of Ocimum basilicum as a natural coagulant for textile wastewater treatment. Industrial Crops and Products, 69, 40–47. https://doi.org/10.1016/j.indcrop.2015.01.045
Sociedad Latinoamericana de Nutrición, H., Sangronis, E., & Unai, E. (2008). Archivos latinoamericanos de nutrición. Archivos Latinoamericanos de Nutrición, 58(1), 64–70. Retrieved from http://www.scielo.org.ve/scielo.php?pid=S0004-06222008000100009&script=sci_arttext&tlng=en
Yin, C. Y. (2010). Emerging usage of plant-based coagulants for water and wastewater treatment. Process Biochemistry, 45(9), 1437–1444. https://doi.org/10.1016/j.procbio.2010.05.030