Actualmente, existe una gran preocupación debido al incremento de la contaminación del agua, el aire y los suelos, causada por las actividades industriales que van en aumento, impactando estos medios de tal forma que los residuos generados exceden la capacidad de carga, lo cual no permite su autodepuración, teniendo como consecuencia la acumulación de tales residuos en el ambiente. Lo anterior, se ve reflejado en el deterioro de la salud pública, disminución de la calidad del agua, el aire, y los suelos, generando problemáticas ambientales a nivel local, regional y global.
Dentro de los residuos más impactantes, se encuentran los metales pesados como el plomo, generado por algunas actividades económicas como la fundición de metales, fabricación de pinturas, equipos electrónicos, industria del vidrio, minería, industrias de petróleo, galvanotecnia, curtiembres y la producción y reciclaje de baterías; siendo esta última una de la que más contamina los cuerpos de agua, teniendo en cuenta que esta industria representa el 80% del uso total del plomo en países donde es medido y registrado (ILZSG, 2010). Un factor muy importante del impacto del plomo en el ambiente, es su capacidad para acumularse en organismos (bioacumulación) y la posibilidad de ascender por la cadena alimentaria (biomagnificación), afectando la integridad de los ecosistemas y la salud de los seres humanos (IPCS, 1995). Además, este elemento es considerado de elevada toxicidad, dado que es embriotóxico, neurotóxico, teratogénico, mutagénico y posiblemente carcinogénico (US-EPA, 2005; ATSDR, 2007). Por esta razón, la eliminación del plomo del ambiente es prioritaria.
Existen varias alternativas de tratamiento tradicionales para la retención de plomo y otros metales pesados, los cuales se clasifican comúnmente en físico-químicos (adsorción, intercambio iónico, procesos de membrana, oxidación avanzada y precipitación química) y biológicos (fitorremediación, bioacumulación, biomineralización, biotransformación y bioadsorción). La bioadsorción, consiste en la capacidad de la biomasa viva o muerta de retener iones metálicos en su superficie, esto es causado, por una serie de interacciones entre la pared de la célula y las especies metálicas presentes en el afluente contaminado (Volesky, 1990; Cañizares, 2000).
Esta investigación, pretende evaluar la capacidad de bioadsorción de plomo (II) de tres bioadsorbentes de origen vegetal, obtenidos a partir de las biomasas: elodea, vaina de arveja y borra del café; mediante pruebas tipo batch en los bioadsorbentes a diferentes concentraciones de Pb(II) y pH en función del tiempo, con los resultados obtenidos en las pruebas se seleccionará el bioadsorbente que presente mayor eficiencia de bioadsorción; finalmente, con el bioadsorbente seleccionado se llevará a cabo una prueba de banco, utilizando una columna de bioadsorción por gravedad, para determinar el tiempo de saturación y de ruptura a partir de la curva de avance, la cual es una representación gráfica del comportamiento del lecho al interior de la columna a medida que desciende el afluente.
2. Materiales y métodos
2.1. Obtención del bioadsorbente.
Los bioadsorbentes vegetales fueron preparados a partir de las biomasas obtenidas de elodea proveniente del lago del parque Metropolitano Simón Bolívar, vainas de arveja de la plaza de mercado de Corabastos y borra del café proveniente de las tiendas de café OMA, en Bogotá Colombia. Las biomasas se lavaron varias veces en un balde con agua potable y luego con agua desionizada. Al finalizar el lavado, se dejó secar cada material al ambiente durante 8 días. Pasado este tiempo, se llevaron a secado en un horno marca Binder a 80ºC por 72 horas. Posteriormente las biomasas fueron molidas en un molino eléctrico marca Corona y tamizadas en tamices marca Dirimpex de 125 µm y 500 µm y finalmente, cada bioadsorbente se empacó por separado en bolsas plásticas herméticas.
2.2. Estudios de bioadsorción en prueba tipo batch
Efecto del pH. Se preparó una solución de Pb (II) con una concentración de 100 mg/l, a partir de nitrato de plomo Pb (NO3)2 marca Merck con un 99.5% de pureza, en agua desionizada; posteriormente, por cada bioadsorbente se prepararon 5 soluciones de 10 mg/l de Pb (II) con pH 3, 4, 5, 6 y 7 respectivamente, agregando 10ml de la solución de 100 mg/l de Pb (II), a cada balón de 100ml y llevándolos al aforo con cada una de las soluciones buffer correspondientes. Por cada bioadsorbente, se realizó un montaje tipo batch en el cual se utilizó un beaker de 250 ml por cada pH, en cada uno de los cuales se adicionó 0.5g de bioadsorbente, con 100 ml de las soluciones preparadas anteriormente. Estos montajes se llevaron a cabo a temperatura ambiente y en agitación constante a 200 rpm en planchas marca Heidolph durante 30 minutos. Pasado ese tiempo se tomaron muestras de 30 ml de las soluciones resultantes en cada beaker y se filtraron mediante un montaje de microfiltración al vacío empleando filtros de membrana marca Schleicher & Schuell de diámetro de poro 0,45 µm. Las muestras se almacenaron en frascos de polietileno, se preservaron con ácido nítrico (HNO3) al 65% (Icontec, NTC 4254, 1997) y fueron analizadas por espectrofotometría de absorción atómica de llama.
2.2.1. Cinética de bioadsorción
Con el fin de poder cuantificar el proceso de bioadsorción, se recurre al cálculo de los parámetros de capacidad de bioadsorción y afinidad de la biomasa por un determinado metal, mediante el ajuste de los datos experimentales a una isoterma de adsorción (Lezcano, 2009). Las isotermas de adsorción son representaciones gráficas de las situaciones de equilibrio entre la concentración del soluto en la fase líquida y la cantidad del mismo que es o no adsorbida por el sólido a una temperatura dada (McCabe, Smith, & Harriot, 2007).
Para cada bioadsorbente, se colocaron en vasos de precipitado de 250 ml, 100 ml de soluciones de 10, 20, 50 y 100 mg/L de Pb (II) respectivamente, ajustadas a pH óptimo; a cada solución se le agregó 0.5g de bioadsorbente. Las soluciones se mantuvieron en agitación constante a 200 rpm y se tomaron alícuotas de 25 ml a los 10, 20, 30 y 45 minutos, las cuales se filtraron, preservaron y analizaron. A cada bioadsorbente se le realizó un control con agua potable y la misma cantidad de bioadsorbente. Para el análisis de los datos obtenidos, se realizaron estudios de cinética de bioadsorción empleando las isotermas de Langmuir y Freundlich con cada uno de los bioadsorbentes. Con los resultados obtenidos, se seleccionó la biomasa vegetal con mayor capacidad de bioadsorción.
2.3. Estudios de bioadsorción en columna
En una columna de bioadsorción, el fluido que se va a tratar, se hace descender a través del lecho empacado a una tasa de flujo constante, entrando en contacto con el bioadsorbente fresco en la parte superior de la columna, donde comienza la bioadsorción progresiva del soluto cada vez que el fluido se va moviendo a través de la columna (Guerrero, 2001). Estos estudios se realizan con el fin de estimar el punto de ruptura al interior del lecho empacado en la columna, el punto de saturación, lo que puede demostrar la capacidad de la columna y en qué momento se debe cambiar de lecho dado que se alcanza el equilibrio de concentraciones con la alimentación de contaminante. El conocimiento de la curva de ruptura, es fundamental para el diseño de columnas de bioadsorción ya que a partir de ella se establecen los parámetros que permitirán predecir el funcionamiento de estos sistemas a mayor escala.
Con el bioadsorbente seleccionado, se realizaron ensayos en una columna de bioadsorción por gravedad, tratando un afluente con las condiciones óptimas encontradas en la etapa anterior. El sistema de columna de bioadsorción consistió en un tanque de alimentación de 20 litros de capacidad, conectado a través de una tubería de PVC de ½“ a una columna de 50 cm de altura y 2,5 cm de diámetro, empacada hasta el 60 % de su altura (previniendo una posible expansión del lecho) con 40 gramos del bioadsorbente seleccionado. La parte inferior de la columna, se unió a una tubería PVC de ½“, que transportó el efluente tratado a un recipiente de recolección. Figura 1.
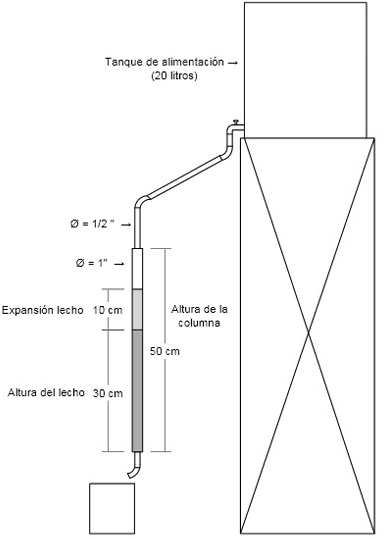
Fig. 1. Montaje columna de bioadsorción
Fuente: autores
Experimentación en columna. Concluida la construcción del sistema de bioadsorción, se hizo circular a través de la columna 2 litros de agua desionizada en un periodo de 24 horas, con el fin de lavar el material bioadsorbente; posteriormente, se hizo circular el afluente sintético, preparado a la concentración y pH óptimos encontrados en la prueba tipo batch. A la salida de la columna se tomaron muestras en función del tiempo, las cuales se almacenaron, preservaron y analizaron. El flujo a través de la columna se midió volumétricamente. Con los resultados obtenidos de las muestras se elaboró la curva de ruptura.
Desorción. Finalizado el ensayo de bioadsorción, la columna fue sometida al proceso de desorción (regeneración). Como regenerante se utilizó una solución de HCl 0,1M (Hernández, 2008; Martínez et al., 2006) cuyo volumen correspondió al 11% del efluente tratado de acuerdo con los antecedentes (Santander, Pávez& Ardiles, 2005). Luego de realizar el proceso de desorción se lavó el bioadsorbente con agua destilada.
3. Resultados y análisis
3.1. Obtención del bioadsorbente.
Después de realizar el tamizado de las biomasas, se obtuvieron tres bioadsorbentes con tamaño de partícula entre 0.125 mm y 0.5 mm, rango que se estableció teniendo en cuenta los estudios realizados por Rabanal (2006) y Hernández (2008), los cuales determinaron que la bioadsorción se ve favorecida utilizando diámetros comprendidos entre 0.1 mm y 0.8 mm.
3.2. Estudios de bioadsorción en prueba tipo batch
Efecto del pH. De acuerdo con los datos obtenidos experimentalmente representados en el gráfico 1, donde se indica el porcentaje de remoción de Pb (II) respecto al pH para cada bioadsorbente, se pudo determinar que el pH que más favorece la bioadsorción en el caso de la elodea y la vaina de arveja es de 4, presentando remociones de 91 y 72,6% respectivamente. Para la borra de café la mayor remoción de Pb (II) se presentó a pH 7, la cual no superó los valores encontrados en los dos bioadsorbentes anteriores con un 68,8%, valor que para efectos de este estudio no es significativo y por lo tanto fue descartado para las siguientes fases.
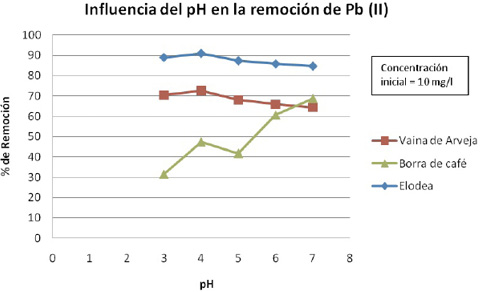
Fig. 2. Influencia del pH en la remoción de Pb (II) en una solución de concentración inicial: 10mg/l
Fuente: autores
Al observar la figura 2 Gráfico 1, se puede apreciar que para los bioadsorbentes elodea y vaina de arveja, la remoción en pH 3 fue ligeramente menor que a pH 4, esto pudo deberse a que en pH 3 la superficie del bioadsorbente estaba desprotonada casi en su totalidad, llegando a su máximo en pH 4 donde sus grupos funcionales con carga negativa (carboxilo, hidroxilo, sulfatos, fosfatos y amino) se encontraban más disponibles, permitiendo la unión con los iones de plomo (II) presentes en la solución. La unión de estos iones a los grupos funcionales, ha sido demostrada por diversos estudios recopilados por Kratochvil & Volesky (1998), donde se evaluó la influencia de los grupos funcionales presentes en hongos, plantas acuáticas y bacterias, concluyendo que estos, son los sitios de unión estratégicos en la superficie del bioadsorbente, cuando se hallan en un rango de pH de 3,5- 5,5. Cabe aclarar que según Lezcano (2009); Naja, Murphy & Volesky (2010) y Hernández (2008), a pH menor a 2, la bioadsorción de iones metálicos se ve inhibida a causa de la alta presencia de protones H+ en la disolución, los cuales compiten por los centros activos en la superficie del bioadsorbente con los iones de plomo, a medida que aumenta el pH ocurre una desprotonación de la superficie que favorece la bioadsorción.
El comportamiento descendente de la remoción de Pb (II) después de pH 4 en elodea y vaina de arveja, teniendo en cuenta que la mayoría de metales pesados, precipitan a pH mayores a 5,5 (Kratochvil & Volesky, 1998), se dio por un posible aumento gradual de la precipitación del catión, formándose hidroxicompuestos como Pb(OH)+, que pudieron afectar la distribución de los iones en la solución disminuyendo la eficiencia de bioadsorción (Lodeiro et al., 2005).
Los porcentajes de remoción de plomo (31,6 % a 68,8 %) en el bioadsorbente borra del café, se vieron afectados, posiblemente, por una obstrucción de los sitios de inserción por parte de los lípidos presentes en su pared celular, que no permitieron la unión de los iones plúmbicos, presentes en la solución a estos sitios; teniendo en cuenta, el contenido de grasas de la borra (26,32%) (Rodríguez, 2009), lo cual le atribuye un carácter lipídico y por ende hidrofóbico al bioadsorbente. Por otra parte, la tendencia a incrementar la remoción a medida que aumentaba el pH, lo cual lo hace diferente frente a los otros dos bioadsorbentes, figura 2, (ver Gráfico 1), pudo deberse a una liberación gradual de los sitios de unión a nivel de la superficie del bioadsorbente con el incremento del pH, gracias a que paulatinamente se hidrolizaron las grasas presentes en la pared celular de la borra, proceso que se completa a pH entre 8 y 9 (Lamarque, 2008).
3.3. Cinética de bioadsorción
En la Tabla 1, se muestra la influencia de la concentración en la remoción de Pb (II) en función del tiempo para los bioadsorbentes, en donde se observa que la bioadsorción fue rápida en todas las concentraciones (10, 20, 50 y 100 mg/l Pb(II)), presentando en los primeros 10 minutos valores de remoción del metal entre 78,41% y 96,21% para el bioadsorbente elodea y entre 60,07% y 90,14% para vaina de arveja, alcanzando el equilibrio a los 30 minutos para la concentración de 20 mg/l en elodea y 100 mg/l en vaina de arveja, en las demás concentraciones no se alcanzó el equilibrio en el tiempo establecido de 45 minutos.
Tabla 1
Resultados obtenidos para las diferentes concentraciones
en función del tiempo.
|
Elodea |
||||||||
|
Concentración* mg/l vs %Remoción |
||||||||
|
10 |
% |
20 |
% |
50 |
% |
100 |
% |
|
|
10 |
2,16 |
78,41 |
0,76 |
96,21 |
2,10 |
95,80 |
6,07 |
93,93 |
|
20 |
1,16 |
88,41 |
0,48 |
97,61 |
1,56 |
96,88 |
5,86 |
94,14 |
|
30 |
0,95 |
90,51 |
0,41 |
97,96 |
1,36 |
97,28 |
6,92 |
93,08 |
|
45 |
0,83 |
91,71 |
0,40 |
97,99 |
1,71 |
96,58 |
6,14 |
93,86 |
|
Vaina de arveja |
||||||||
|
Tiempo (min) |
Concentración* mg/l vs %Remoción |
|||||||
|
10 |
% |
20 |
% |
50 |
% |
100 |
% |
|
|
10 |
1,07 |
89,26 |
2,58 |
87,08 |
19,96 |
60,07 |
9,86 |
90,14 |
|
20 |
1,79 |
82,06 |
2,00 |
89,98 |
7,97 |
84,05 |
11,46 |
88,54 |
|
30 |
2,80 |
71,96 |
1,41 |
92,93 |
6,91 |
86,17 |
18,96 |
81,04 |
|
45 |
1,87 |
81,26 |
1,27 |
93,63 |
5,68 |
88,63 |
18,96 |
81,04 |
|
*A todas las concentraciones finales se les resto el aporte del control de cada bioadsorbente: |
||||||||
Fuente: autores
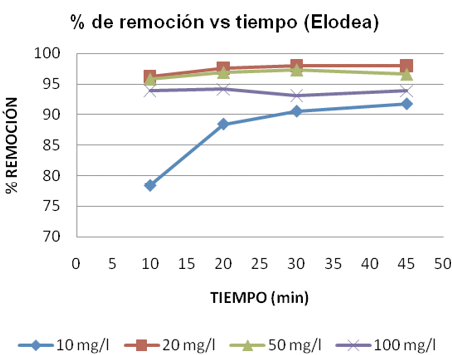
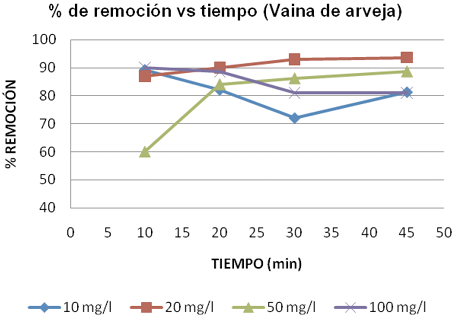
La rapidez del proceso de bioadsorción pudo deberse principalmente, a que la fijación del metal se lleva a cabo a través de reacciones rápidas y reversibles que ocurren en la superficie del bioadsorbente y que tienen lugar en ausencia del metabolismo (Lezcano, 2009). Adicionalmente, las figuras 3 y 4, indican que para los bioadsorbentes elodea y vaina de arveja, la concentración de 20 mg/l fue la que presentó mayores porcentajes de remoción a los 45 minutos, con un 97,99 y 93,63% respectivamente. En esta concentración también es notable un descenso de la cantidad del metal a medida que aumenta el tiempo.
 (a)
(a) 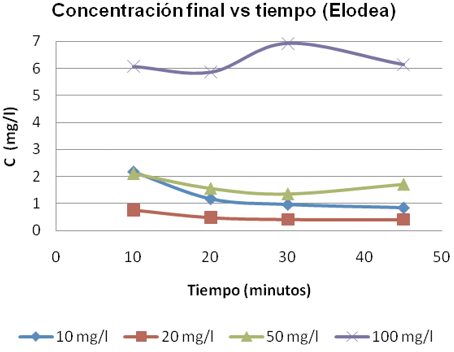 (b)
(b)
Fuente. autores
 (a)
(a)
 b)
b)
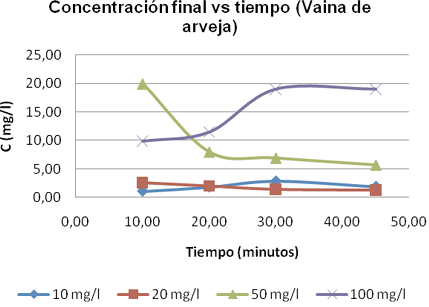
Fig. 3. Influencia de la concentración en la remoción de Pb (II)
a través del tiempo (Vaina de arveja).
Fuente: autores
En la elodea, salvo pequeñas diferencias, todos los porcentajes de remoción están por encima del 90% lo cual refleja su alta eficiencia de remoción de Pb (II), incluso a mayores concentraciones. En el caso de la vaina de arveja la mayoría de los valores no superan esta remoción, sin embargo, estos resultados pueden considerarse también altos.
Considerando los anteriores resultados, se estableció que la concentración óptima para la bioadsorción es de 20 mg/l a pH 4, a partir de la cual se elaboraron las isotermas de Langmuir y Freundlich, con el fin de determinar los parámetros que cuantifican el proceso.
- • Isotermas de Langmuir y Freundlich
 (a)
(a)
 (b)
(b)
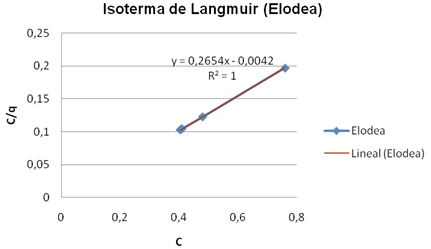
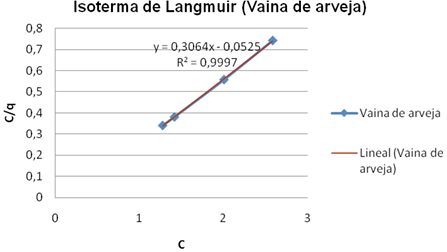
Fig. 4. Isoterma de Langmuir para la Elodea y vaina de arveja. Fuente: autores
A partir de la regresión lineal de los gráficos 4a y 4b se obtuvieron las constantes de Langmuir (qmax y K), encontrando que la capacidad de bioadsorción (qmax) para la elodea fue mayor respecto a la vaina de arveja, siendo de 3,768 mg de Pb (II)/g de bioadsorbente y 3,264 mg/g respectivamente, no obstante, la afinidad del bioadsorbente con el plomo (K) fue mucho mejor para la elodea que para la vaina de arveja presentando valores de 0,016 mg/l frente a 0,171 mg/l, teniendo en cuenta que entre más pequeño sea K, mayor es la afinidad (Lezcano, J. 2008; Volesky, B. 2003).
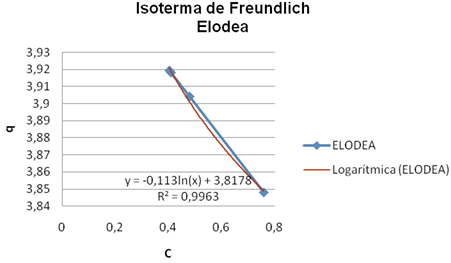
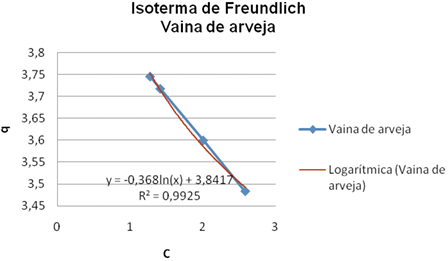
La isoterma de Freundlich se determinó para cada uno de los bioadsorbentes, con el fin de comparar el coeficiente de determinación de esta con la del modelo de Langmuir, el R2 para el modelo de Freundlich, se determinó a partir de la regresión logarítmica de las figuras 5a y 5b.
 (a)
(a)
 (b)
(b)
Fig. 5. Isoterma de Freundlich para la elodea y vaina de arveja. Fuente: autores.
Los valores del coeficiente de determinación (R2) que miden el grado de ajuste de los datos a los modelos de Langmuir y Freundlich para cada bioadsorbente, indican que los modelos se ajustaron perfectamente a los datos experimentales, siendo la elodea la que mejor se ajustó con un R2 en Langmuir de 1 y 0,9963 en Freundlich y la vaina de arveja 0,9997 y 0,9925 respectivamente. Los coeficientes de determinación en el modelo de Langmuir, indican que la variación de los valores de la relación C/q son explicados perfectamente por C, para ambos bioadsorbentes (100% elodea y 99,97% vaina de arveja); en cambio, en Freundlich la variación de los valores de q se explica casi en su totalidad por la variable independiente (C) (99,63% elodea y 99,25%). Con base en el alto grado de ajuste que presentaron los modelos, se puede afirmar que la ecuación de regresión obtenida, sirve de herramienta para efectuar predicciones y estimaciones del comportamiento de la bioadsorción para los bioadsorbentes estudiados.
3.4. Experimentación en columna
Para el estudio de columna se utilizó como bioadsorbente la elodea ya que presentó los mayores porcentajes de remoción de plomo y se trabajó con los parámetros óptimos seleccionados en las pruebas anteriores (pH 4 y concentración de 20 mg/l).
Partiendo del valor de qmax (3,768 mg Pb(II)/ g bioadsorbente), obtenido en la isoterma de Langmuir para elodea a una concentración afluente de 20 mg/l y de la masa de lecho empacado (40 gramos de bioadsorbente elodea), se definió el volumen de agua a tratar, el cual dio un valor de 7,5 litros, cantidad aproximada necesaria para llegar al punto de saturación. En este sentido, se hizo pasar a través de la columna, el volumen de afluente sintético estimado a una concentración inicial (Co) de 20 mg/l de plomo (II) a pH 4, durante 40 horas; con un caudal (Q) constante de 189 ml/h, medido volumétricamente, y a una velocidad de 38,50 cm/h. En el transcurso de la experimentación en columna, se pudo notar que el lecho se expandió 10 cm, debido, probablemente, a la capacidad de las partículas del bioadsorbente elodea para absorber agua, lo que implica que el diámetro de partícula aumente; esta característica, resulta ser importante para futuros diseños de columna, ya que se hace necesario dejar un espacio libre al interior de la misma que permita la expansión del lecho.
La Tabla 2, muestra los datos obtenidos a partir de la experimentación en columna, producto de la medición de la concentración final (C) en función del tiempo (t).
Tabla 2
Datos obtenidos a partir de la experimentación en columna.
|
Tiempo (horas) |
C (mg/l) |
Co (mg/l) |
C/Co |
|
4 |
0,049 |
20 |
0,0025 |
|
8 |
0,049 |
0,0025 |
|
|
12 |
0,049 |
0,0025 |
|
|
16 |
0,049 |
0,0025 |
|
|
20 |
0,049 |
0,0025 |
|
|
24 |
0,049 |
0,0025 |
|
|
28 |
0,066 |
0,0033 |
|
|
30 |
0,100 |
0,0050* |
|
|
32 |
0,133 |
0,0067 |
|
|
36 |
0,202 |
0,0101 |
|
|
40 |
0,287 |
0,0144 |
* Punto de ruptura, hallado por interpolación.
Fuente: autores
El punto de ruptura para este ensayo, se estableció como CR/Co = 0,005, para una concentración de ruptura (CR) de 0,1 mg/l (ver tabla 2); teniendo en cuenta, que este valor es el límite máximo permisible para plomo en aguas residuales, fijado en las normas: la resolución 3957 de 2009 y la resolución 631 de 2015. El tiempo de ruptura (tR), se halló por interpolación de los datos de la Tabla 2, resultando un tR = 30 horas. La figura 6, representa la curva de ruptura, donde la relación de concentraciones (C/Co) se grafica en función del tiempo; en esta se observa que en un tiempo dado de 24 horas, cuando casi la mitad del lecho está saturada de soluto (Geankoplis, C. 1999), la concentración de salida sigue siendo menor a 0,049, hasta que la zona de transferencia de masa empieza a llegar a la salida de la columna a las 28 horas. Entonces, la concentración de salida empieza a elevarse, y a las 30 horas, llega al punto de ruptura (CR/Co). Después de que se alcanza dicho punto, la concentración final (C), tiende a elevarse progresivamente en los tiempos 32, 36 y 40 horas; presentándose concentraciones de 0,133 mg/l; 0,202 mg/l y 0,287 mg/l de Pb (II) respectivamente.
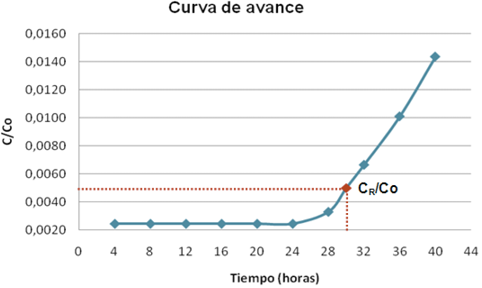
Fig. 6. Curva de avance, para la columna empacada con elodea.
Fuente. autores
El valor del punto de ruptura, resulta ser de gran importancia en la toma de decisiones, en vista de que a partir de este punto, las concentraciones de salida aumentan sobrepasando el límite máximo permisible (0,1mg/l), lo que permitiría definir, en qué momento se debe interrumpir el flujo y trasladar el afluente a otro lecho fresco o regenerado, o bien recircular el efluente, aunque este último, no es recomendado teniendo en cuenta que en este punto la mayor parte de la capacidad del lecho ha sido usada (Ibíd. p. 779).
Para efectos de este ensayo, no fue posible alcanzar el punto de saturación del lecho bioadsorbente elodea, probablemente, a que la naturaleza de los datos estimados pueden ser inexactos a causa de muchas incertidumbres, debidas a los patrones de flujo (pistón, slug, burbuja, transición y anular), la dispersión axial del fluido (distribución del flujo al interior del lecho) y la resistencia a la transferencia de masa por parte del lecho (McCabe, W.; Smith, J. y Harriot, P. 2007); lo que pudo llevar a un aumento del tiempo de saturación (>40 horas) y por ende sería necesario tratar mayor cantidad de afluente.
3.5. Desorción.
Finalizado la experimentación en columna, se realizó la desorción durante 4,3 horas aproximadamente, utilizando como desorbente 825 ml de HCl 0,1 M, correspondientes al 11% del efluente tratado (7,5 litros), obteniendo una remoción del 60,6% de plomo retenido en el lecho. Lo cual indica que el volumen de desorbente empleado en este ensayo, no fue suficiente para lograr una remoción del 100%. No obstante, este porcentaje de remoción, indica que este desorbente podría aumentar su eficiencia, incrementando el volumen del mismo.
4. Conclusiones
En la prueba tipo batch para la evaluación del pH, se comprobó que el pH óptimo encontrado para los bioadsorbentes elodea y vaina de arveja fue 4, presentando porcentajes de remoción del orden de 91% y 72,6% respectivamente. En la evaluación de la concentración, se encontró que a 20 mg/l la elodea presentó una mejor remoción (97,99%) frente a la vaina de arveja (93,63%) a los 45 minutos.
En la experimentación en columna, el punto de ruptura (CR/Co= 0,005) se alcanzó en un tiempo de 30 horas, para una concentración de ruptura (CR) de 0,1 mg/l, a partir de este punto, la concentración de salida aumentó paulatinamente, pero no se alcanzó el punto de saturación a las 40 horas como se había estimado con los datos de qmax.
El Pb (II) retenido en el lecho, fue desorbido en un 60,6% utilizando como desorbente 825 ml HCl 0,1M, mostrando que este volumen no fue suficiente para remover el 100% del metal.
En este estudio se demostró que la elodea es un bioadsorbente efectivo para la remoción de Pb (II) presente en aguas contaminadas, lo que podría convertirlo en una alternativa novedosa y viable para el tratamiento de aguas industriales.
Referencias
Agency for Toxic Substances and Disease Registry (ATSDR). (2007), Toxicological Profile for Lead, Department of Health and Human Services, pp. 29-47. USA.
Cañizares, R. (2000), Bioadsorción de metales pesados mediante el uso de biomasa microbiana., Revista Latinoamericana de Microbiología, vol. 42, pp. 131-143.
Geankoplis, C. (1999), Procesos de transporte y operaciones unitarias., Ingra Mex. S.A. (ed.), México, pp. 773-783.
GUERRERO, J. (2001). Tratamiento de aguas residuales. Bogotá: Universidad Nacional Abierta y a distancia (UNAD), pp. 630 – 665.
Hernández, A., Miralles, N. (2008). Influencia del tamaño de partícula en la bioadsorción de plomo con raspo de uva., tesis presentada a la Universidad Politécnica de Cataluña, para optar al grado de maestría.
Instituto Colombiano de Normalización y Certificación. (1997), Gestión ambiental, Calidad del agua: determinación de Co, Ni, Cu, Zn, Cd y Pb. Métodos espectrométricos de absorción atómica de llama., NTC 4254, Bogotá D.C, pp. 2-10 p.
International Lead and Zinc Study Group (ILZSG). (2010), End uses of lead and zinc.
International Programme on Chemical Safety (IPCS). (1995), Environmental Health Criteria 165: Inorganic Lead, Geneva, World Health Organization (WHO).
Kratochvil, D., Volesky, B., (1998), Advances in the biosorption of heavy metals, Journal Trends in Biotechnology, vol. 16, No. 7, pp. 291-300.
Lamarque, A., (2008), Fundamentos teórico-prácticos de química orgánica, Brujas (ed.), Argentina, pp. 116.
Lezcano, J., (2008), Efecto del pretratamiento de biomasa procedente de un hábitat eutrofizado sobre la bioadsorción de metales pesados, tesis presentada a la Universidad complutense de Madrid, para optar al título de Doctor en Biología.
Lodeiro, P., Cordero, B., Barriada, J.L., Herrero, R., Sastre de Vicente, M. E., (2005), Biosorption of cadmium by biomass of brown marine macroalgae, Journal Bioresource Technology, Vol. 96, No. 16, pp. 1796-1803.
Martínez, M., Miralles, N., Hidalgo, S., Fiol, N., Villaescusa, I., Poch, J., (May. 2006), Removal of lead (II) and cadmium(II) from aqueous solutions using grape stalk waste, Journal of Hazardous Materials. Vol. 133, No. 3, pp. 203-211.
McCabe, W., Smith, J., Harriot, P., (2007), Operaciones unitarias en ingeniería química. 7 ed. McGraw Hill, México, pp. 880-897.
Naja, G., Murphy, V., and Volesky, B., (2007), Biosorption, metals, Journal Wiley Encyclopedia of Industrial Biotechnology, pp. 2 - 48.
Rabanal, M., (2006). Estudio de la biosorción de Co (II) por el alga marina Macrosystis pyrifera., tesis presentada a la Universidad Nacional Mayor de San Marcos, para optar al título de químico. Lima.
Rodríguez, A., Letón P., Rosal, R., Dorado, M., Villar, S., Sanz J.M., (2006). Tratamientos avanzados de aguas residuales industriales. Informe de vigilancia tecnológica. Madrid, España., Universidad de Alcalá. Círculo de Innovación en Tecnologías Medioambientales y Energía (CITME), pp. 24–26.
Rodríguez, N., (2009), Estudio de un biosistema integrado para el postratamiento de las aguas residuales del café utilizando macrófitas acuáticas., tesis presentada a la Universidad politécnica de Valencia, para optar al grado de Doctor.
Santander, M., Pávez, O., Ardiles A., (2005). Bioadsorción de Iones Cobre en Biomasa Vegetal Deshidratada, Revista de la facultad de Ingeniería, Universidad de Atacama. Vol. 19, pp. 11-15.
U.S. Environmental Protection Agency (EPA), (2005). Lead in Paint, Dust and Soil Recent. United States., EPA.
Volesky, B., (1990), Biosorption of Heavy Metals. CRC Press (ed.), Florida, pp. 3-65.
Volesky, B., (2003), Sorption and Biosorption. BV-Sorbex, Inc (ed.), Montreal, Canada, pp. 103-115.